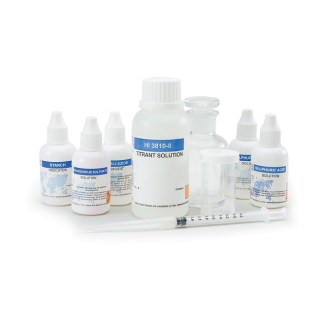
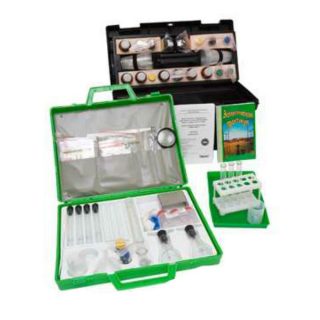
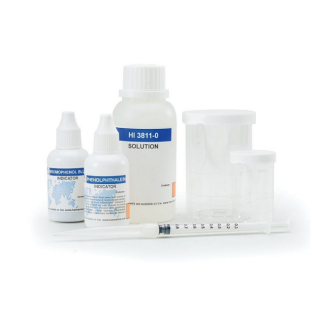
HI3810 представляет собой набор химических реагентов для определения содержания растворённого кислорода с помощью модифицированного метода титрования Винклера. HI3810 поставляется в комплекте со всеми реагентами и оборудованием, необходимыми для выполнения примерно 110 тестов.
- Готовые реактивы для удобства использования
- На всех реагентах указан срок годности и номер партии
- Титрование с крахмалом в качестве индикатора
Особенности HI3810:
-
Полный комплект
-
В состав набора химических реагентов включены все необходимые материалы, такие как стеклянная бутылка с притёртой пробкой, индикатор и бутылки с реагентами, а также мерный шприц.
-
-
Высокое разрешение
-
Значения от 0 до 10 мг/л определяются с разрешением до 0,1 мг/л.
-
-
Наличие сменных реагентов
-
Когда реагенты закончатся, то нет никакой необходимости покупать новый комплект. Для возмещения входящих в комплект реагентов, можно заказать набор HI3810-100.
-
Важность использования
Концентрация растворённого кислорода в воде чрезвычайно важна как в природе, так и в человеческом окружении. В океанах, озерах, реках и других поверхностных водных объектов, растворённый кислород имеет важное значение для роста и развития водной флоры и фауны. Без кислорода вода может стать токсичной вследствие анаэробного гниения органического вещества. В человеческом окружении, вода должна содержать, по меньшей мере, 2 мг/л кислорода для защиты водопроводных труб от коррозии. Тем не менее, во многих случаях, котловая вода не может содержать более 10 мг/л кислорода.
В тестовом наборе HI3810 используется модифицированный метод Винклера. Ионы двухвалентного марганца реагируют с кислородом в присутствии гидроксида калия с образованием осадка оксида четырёхвалентного марганца (стадия 1). С целью предотвращения мешающего влияния нитрит ионов, в состав реагента добавлен азид. При добавлении кислоты, оксид гидроксид марганца окисляет йодид в йод (стадия 2). Так как количество образовавшегося йода эквивалентно содержанию кислорода в образце, концентрация йода рассчитывается при титровании тиосульфатом, восстанавливающим йод обратно в ионы иодида (стадия 3).
- Стадия 1: 2Mn2+ + O2 + 4OH— → 2MnO(OH)2
- Стадия 2: MnO(OH)2 + 2I— + 4H+ → Mn2+ + I2 + 3H2O
- Стадия 3: I2 + 2S2O32— + S4O62-